钾(K)、钙(Ca)是太阳系和地球的重要组成元素,也是人体和其他生命体内必需的营养元素。钾是生命体细胞内最富集的金属阳离子,钙是人体骨骼和牙齿的主要组成元素,它们参与多种重要的生理过程,如维持细胞渗透压平衡、参与蛋白质和能量代谢、维持神经传递的正常功能、维持正常的肌肉收缩等。近年来,随着多接收等离子体质谱仪(MC-ICP-MS)技术的发展,使获得高精度钾、钙稳定同位素成为了可能,尤其是配备碰撞池的新型仪器能够消除钾、钙同位素测定过程中同质异位素的干扰。然而,目前关于钾、钙同位素在生命科学上的应用分别集中于对植物和骨钙平衡的研究,严重缺乏关于不同器官中钾、钙稳定同位素组成及其分馏机制的研究工作。因此,探究不同器官中钾、钙稳定同位素组成特征对深入理解生命体中钾、钙循环及生命体的健康具有重要意义。
针对上述问题,中国科学院地质与地球物理研究所博士研究生崔梦萌、导师苏本勋研究员与法国巴黎地球物理研究所Frédéric Moynier教授团队合作,利用碰撞反应池MC-ICP-MS(Nu Sapphire)对不同性别、基因学背景的10只小鼠体内不同器官(包括大脑、骨骼、肝脏、肾脏、肌肉、血液)开展了高精度钾、钙稳定同位素分析测试工作,取得主要认识如下:
(1)小鼠不同器官之间钾稳定同位素分馏高达约2‰,大脑和红细胞之间具有最大的钾同位素差异,其中大脑富集轻钾同位素(δ41K = -1.13~-0.09 ‰)而红细胞富集重钾同位素(δ41K = 0.67~0.08 ‰)。相比于大脑和红细胞,肝脏、肾脏和肌肉中的钾同位素差异较小,平均δ41K值分别为-0.12 ± 0.58 ‰、-0.24 ± 0.57 ‰和0.01 ± 0.53 ‰(图1)。通过分析不同因素对小鼠不同器官之间钾同位素组成差异的影响,发现不同性别及基因学背景差异对钾同位素影响较小,而不同器官的自身特性差异是控制钾同位素分馏的主要因素。此外,大脑和红细胞的钾同位素呈现较好的相关性,表明大脑中钾的消耗直接影响血液中的钾(图2)。因此,可通过检测容易获得的血液样本中钾同位素组成特征来分析大脑中钾同位素的变化,以此来为研究与钾失衡相关的大脑疾病(如阿尔茨海默病)提供一定的指示意义。
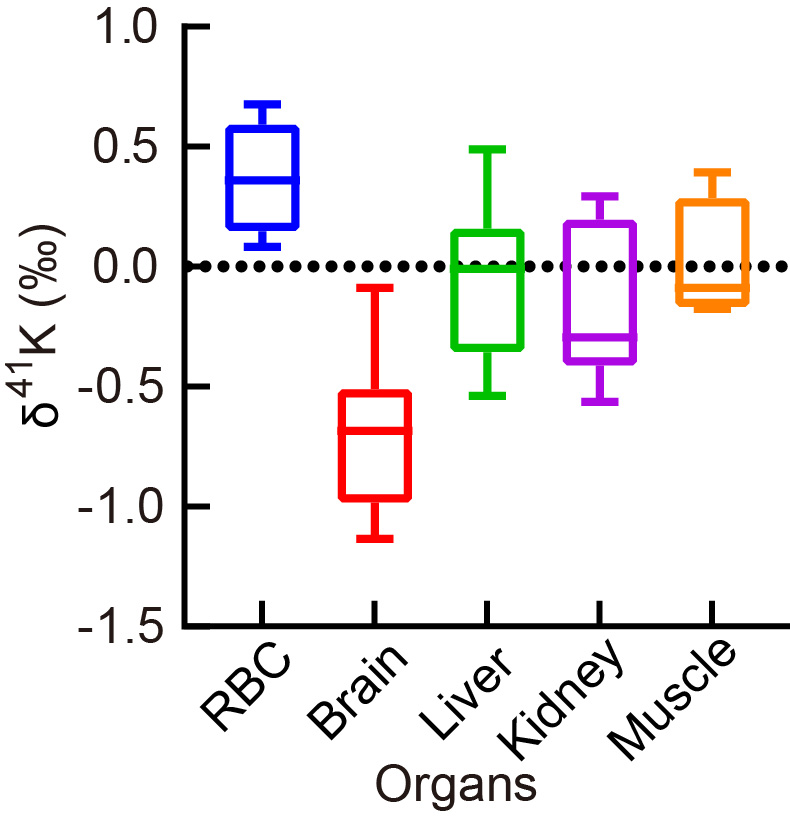
图1 小鼠不同器官中钾同位素组成特征
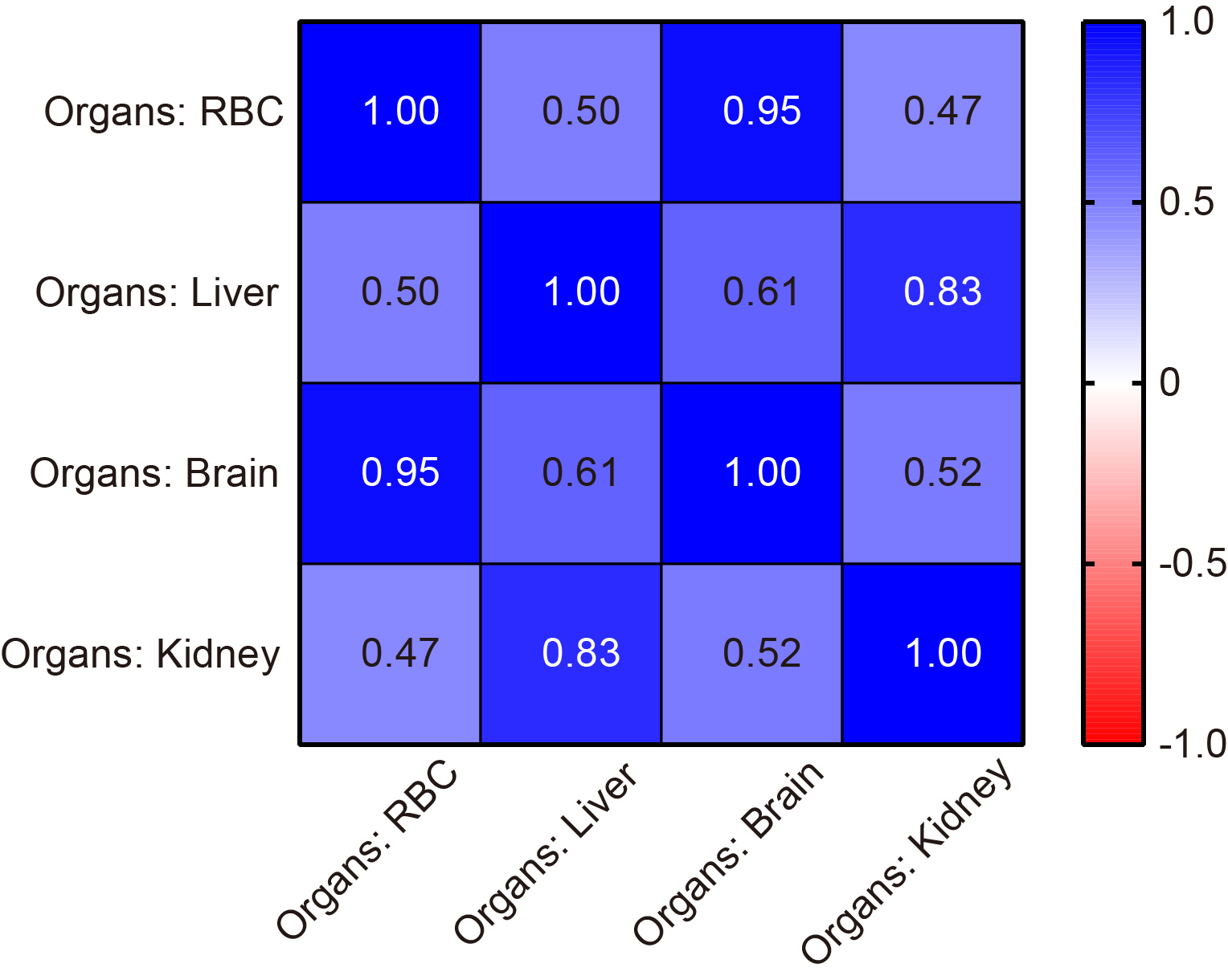
图2 小鼠不同器官中钾同位素的斯皮尔曼相关性热力图
(2)小鼠不同器官之间钙稳定同位素分馏可达约1‰(图3),其主要受控于不同器官之间的钙代谢差异,而与性别和基因学背景的差异无关。相比于血液和其他软组织(肝脏、肾脏、肌肉),骨骼明显富集轻钙同位素(δ44/40Ca = 0.10 ± 0.55‰),表明骨形成过程中优先吸收轻钙同位素。肾脏相比于血液富集重钙同位素(δ44/40Ca = 0.86 ± 0.31‰),表明肾脏代谢过程中只有较少部分的重钙同位素进入尿液,而大部分重钙同位素经重吸收作用进入血液参与其他生理过程。相对于其他器官,大脑具有异常轻的钙同位素组成(δ44/40Ca = 0.10 ± 0.53‰),表明具有轻钙同位素特征的游离钙离子在动力学同位素效应下优先从血液进入大脑中(图4)。这些特征揭示了钙同位素在研究钙失衡相关疾病(如阿尔茨海默病、骨质疏松、肾结石等)方面的巨大潜力。

图3 小鼠不同器官中钙同位素组成特征

图4 小鼠不同器官之间的钙同位素运输模型
该研究系统地分析了小鼠不同器官中钾、钙稳定同位素组成特征,并分析了造成其同位素差异的主要因素,为今后利用钾、钙稳定同位素研究人体健康提供了参考,同时也推动了金属稳定同位素在生命科学领域的发展。
研究成果发表于国际学术期刊Metallomics和Analytical and Bioanalytical Chemistry,该研究受法国国家科学研究中心(CNRS)横向和跨学科创新任务(MITI)、巴黎地球物理研究所(IPGP)多学科项目(PARI)共同资助。
1. 崔梦萌,Frédéric Moynier,苏本勋,戴维,胡妍,Dimitri Rigoussen,Brandon Mahan,Marie Le Borgne. Stable potassium isotope distribution in mouse organs and red blood cells: implication for biomarker development[J]. Metallomics, 2023, 15(7): 1-11. DOI: 10.1093/mtomcs/mfad033.
2. 崔梦萌,Frédéric Moynier,苏本勋,戴维,Brandon Mahan,Marie Le Borgne. Distinctive calcium isotopic composition of mice organs and fluids: implications for biological research[J]. Analytical and Bioanalytical Chemistry, 2023, 415: 6839-6850. DOI: 10.1007/s00216-023-04962-7.

