氨氧化奇古菌(Ammonia-oxidizing archaea,AOA)是地球海洋中最丰富的微生物之一,占海洋中浮游微生物的30%,在海洋的氮循环和碳循环中发挥着关键作用。氨氧化奇古菌可以在有氧条件下将氨氧化为亚硝酸盐(NH3 + 1.5O2 → NO2-+ H2O + H+)。古菌中氨氧化生理功能的发现极大地改变了人们对全球氮循环的认识。系统基因组学和分子钟分析表明,可以进行氨氧化的古菌可能在10亿年前就已经出现。现代环境中的氨氧化奇古菌展现出对深海低营养和低能量通量环境非凡的适应能力,它们具有高效的有氧固碳能力,也被认为是温室气体N2O的主要来源之一。然而,氨氧化奇古菌在缺氧环境(比如 海洋最低含氧区,图1)中的存在以及其生理和代谢机制仍然令人困惑。
海洋最低含氧区,图1)中的存在以及其生理和代谢机制仍然令人困惑。

图1 海洋最低含氧区示意图(修改自Martens-Habbena et al., 2022)
最近,Kraft等利用高灵敏度氧传感器研究了氨氧化奇古菌Nitrosopumilus maritimus在氧气浓度较低的环境中的代谢过程。他们发现当O2被消耗到1 nM后,体系中的O2开始缓慢增加(图2),并且O2的产生还伴随着 N2的生成。为了探究N. maritimus在产氧的同时是否会继续氧化氨,Kraft等通过同位素标记法(15N-NH4+)对氨转化为亚硝酸盐的过程进行了示踪。实验结果表明,N. maritimus在产氧的过程中,氨也被氧化为亚硝酸盐。并且,N. maritimus产生的大部分氧气都立即被氨氧化消耗掉。
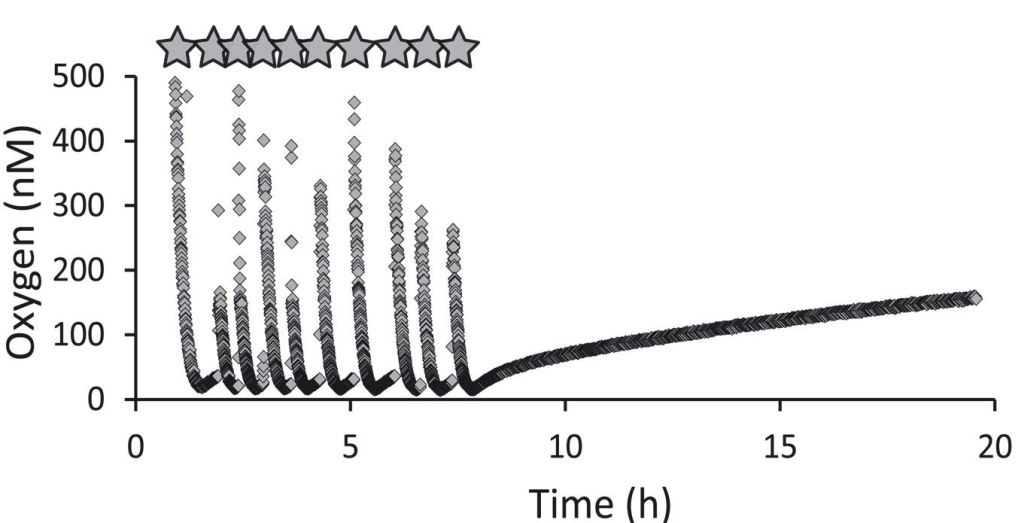
图2 氨氧化奇古菌N. maritimus的产氧过程。氧气被消耗后,体系中氧浓度立即开始增加(0至8小时)。当N. maritimus的培养过程不受干扰且不添加含氧水时,氧气浓度会随着时间的推移而继续增加(8至20小时)(Kraft et al, 2022)
前人虽然提出了三种非光合产氧的途径:亚氯酸盐的歧化反应(ClO2-→Cl- + O2)、活性氧物质的降解(例如 H2O2 的歧化反应H2O2→H2 + O2)和一氧化氮(NO ) 的歧化反应(2NO2- → 2NO →N2+O2)。由于N. maritimus的培养基中不包括高氯酸盐、氯酸盐或亚氯酸盐,排除了亚氯酸盐歧化反应的可能性。并且,Kraft等通过在培养基中添加丙酮酸,也排除了H2O2通过歧化反应产生氧气的可能性(丙酮酸可以与H2O2发生脱羧反应)。由于N. maritimus在正常有氧条件下进行氨氧化时可以产生NO,因此NO可能是N. maritimus产氧的重要中间产物之一。但是同位素标记(15N-NO2-)实验发现,在N. maritimus培养的前20小时内,O2和N2的产出是不耦合的,这说明在NO转变为N2和O2之间还存在着进一步的中间产物。Kraft等推测这个中间产物可能是 N2O(2NO→N2O + 0.5O2),这也得到了反应速率测量和同位素标记实验结果的支持:N2和 N2O 的产出速率与O2 的产出速率在误差范围内一致;以15N-亚硝酸盐为底物培养N. maritimus的过程中,46N2O比30N2的产出更早(图 3A和B)。并且,同位素标记实验结果表明,N. maritimus生成的N2O全部来自于亚硝酸盐(图 3B)。
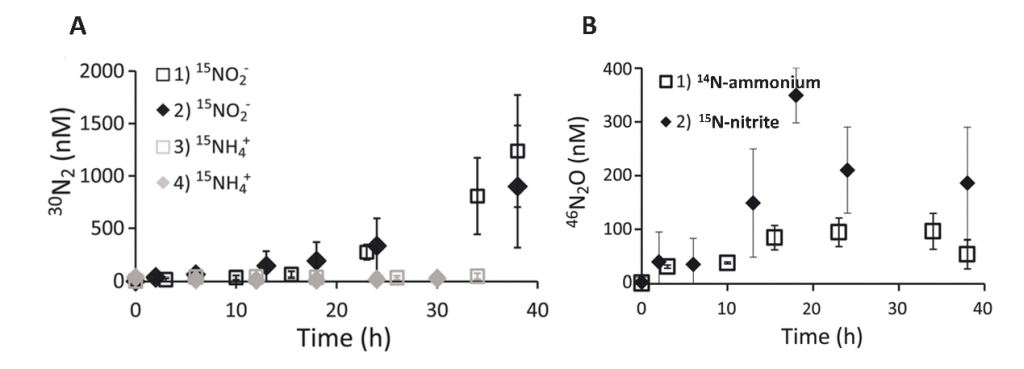
图3 以15N-亚硝酸盐(15N-NO2-)或15N-铵(15N-NH4+)为底物培养氨氧化奇古菌N. maritimus产生的30N2(A)。以14N-铵(14N-NH4+)或15N -亚硝酸盐(15N-NO2-)为底物培养氨氧化奇古菌N. maritimus产生的46N2O(B)(修改自Kraft et al, 2022)
目前已知的NO歧化反应只发生在NC10菌群中,其歧化反应产生的氧气用于甲烷的氧化。由于NC10菌群中氧气的产生和消耗是紧密耦合的,因此NC10菌群无法将自由氧释放到环境中。N2O中间产物的生成将N. maritimus的代谢机制与 NC10 细菌的代谢机制区分开来,后者生成O2的过程中不需要N2O作为中间产物。由于缺乏生化方面的先例,Kraft等根据细胞数量、速率测量和同位素分析的实验结果,提出了N. maritimus产生氧气和氮气的代谢途径(图4)。(1)氨氧化途径(灰色):氧气通过氨单加氧酶(ammonia monooxygenase,AMO)激活氨氧化,氧化NH4+的两个电子进入电子转移链,并被转移到末端氧还原酶从而还原O2。(2)产氧途径(黑色):亚硝酸盐被亚硝酸盐还原酶NirK还原为NO。NO通过歧化反应生成O2和N2O。累积的O2在氨氧化过程中被消耗,而N2O则被进一步还原为N2。但是目前N. maritimus中的N2O还原酶尚未可知。
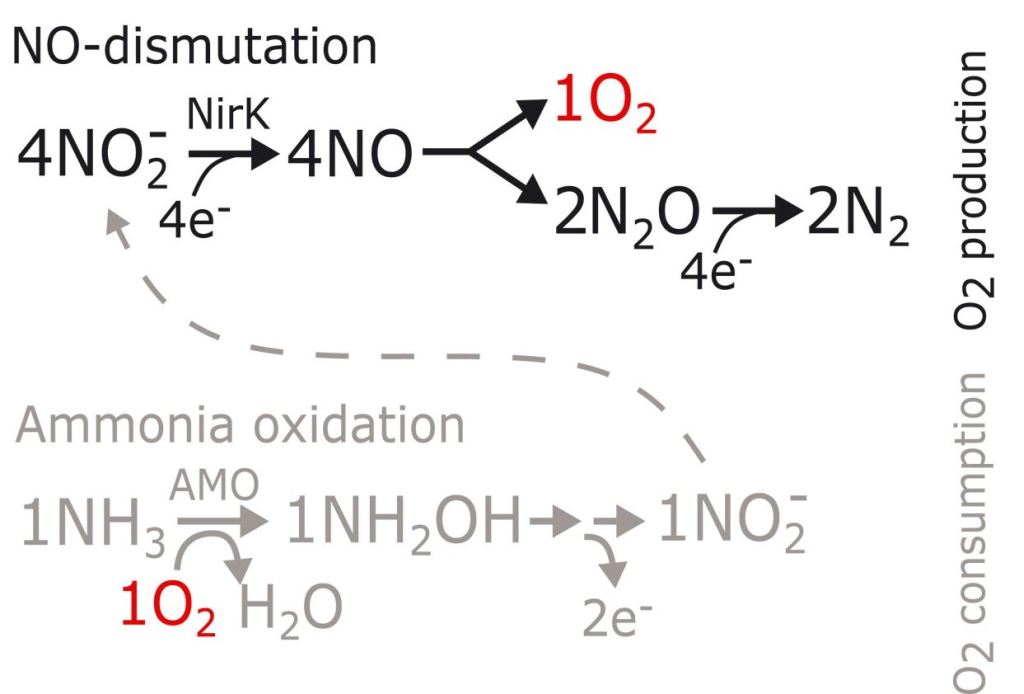
图4 N. maritimus产生氧气和氮气的代谢途径(Kraft et al, 2022)
综上所述,Kraft等人证实了氨氧化奇古菌N. maritimus在缺氧条件下,不仅可以产生用于自身氨氧化的O2,同时可以将亚硝酸盐还原为N2,这是一种新的N2的产生途径。氨氧化奇古菌与亚硝酸盐氧化细菌(nitrite-oxidizing bacteria,NOB)共同为海洋提供了主要的无机氮源(图5)。N. maritimus作为少数几种已知能在黑暗中产生氧气的生物之一,为氨氧化奇古菌在海洋最低含氧区的存在提供了解释。考虑到全球海洋中氨氧化奇古菌的丰度及其在氮循环中的关键作用,氨氧化奇古菌的产氧过程可能对缺氧环境中微生物的生态体系和元素的生物地球化学循环具有深远的意义。
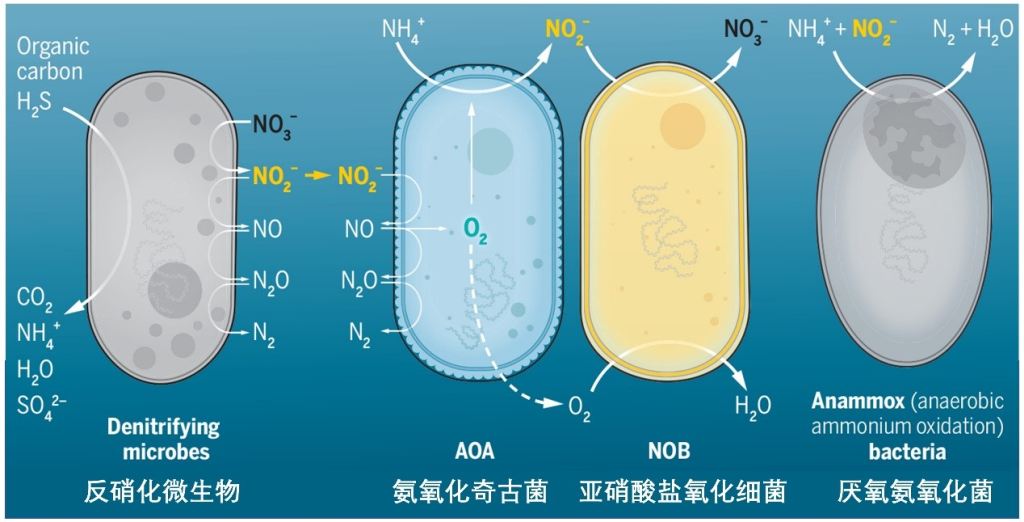
图5 氨氧化奇古菌(AOA)和亚硝酸盐氧化细菌(NOB)在海洋最低含氧区氮循环中的作用示意图(修改自Martens-Habbena et al., 2022)
主要参考文献
Kraft B, Jehmlich N, Larsen M, et al. Oxygen and nitrogen production by an ammonia-oxidizing archaeon[J]. Science, 2022, 375: 97-100.(原文链接)
Martens-Habbena W and Qin W. Archaeal nitrification without oxygen[J]. Science, 2022, 375:27-28.
(撰稿:韩晓华/地星室)

